一、导语
很多企业常常会遇到这些情况,内控体系建立后,得到一本手册,一阵忙碌和热闹之后,高高举起,又轻轻放下。内控手册有了,内控流程有了,那这些管理流程具体应该怎么落实执行呢?这需要我们的管理部门结合企业的实际运营情况,进一步细化管理制度,确保既能满足业务规范性,又能应对内控风险,使得公司运营更加合规。就像治沙一样,大家都知道种树可以治沙,但是种什么树,从哪里开始种,就需要我们根据土壤的实际情况,水源的分布情况来确定。
二、制度应以内控为框架进行补充完善
对于未曾全面开展内控体系建设的企业而言,自身已有的制度文件其实并不少,但是也会面临这些问题:制度散落在各个部门,员工不便查找;或者公司明明好几百个制度,还是觉得核心业务制度缺失。那么如何通过制度建设解决这些问题呢?为了将内控落到实处,需要通过制度将控制措施细化,梳理流程具体的操作要求和标准。通常,企业应该通过内控手册进行制度对标,将制度和控制措施联系起来,让制度细化控制措施。制度的完善应以内控体系作为依据,针对现有的制度查漏补缺,并对其进行补充完善。制度就是文字化的内控流程图,制度的编制应以内控流程图的主要流程步骤为整体框架,对每个控制措施进行细化和补充,详细规定该控制措施的实施主体、主体权限、具体举措、输出单据等。以制度的覆盖率作为制度完善程度的量化标准和管理提升的体现。
总之,制度应以内控为框架进行补充和完善,企业应通过制度覆盖率来量化制度建设情况,并通过制度覆盖率变化情况的统计和分析,逐步提升管理水平。
三、制度要厘清责任
企业的各个部门往往清楚自己部门的职责是什么,但是其他部门要配合做什么或者要配合其他部门做什么,却并不明确,因此形成了部门间的壁垒。管理部门通常负有对流程规范的制定,流程执行的监督,流程质量的提升等相关职责。内控的作用之一就是要打破部门间的壁垒,厘清各部门的职责。当然对于这些职责,同样需要通过制度将其补充完善,明确部门内部的责任,主责部门的责任,协助部门的责任,领导的责任。
通常编写时我们采用5W1H方法,来明确职责和要求:
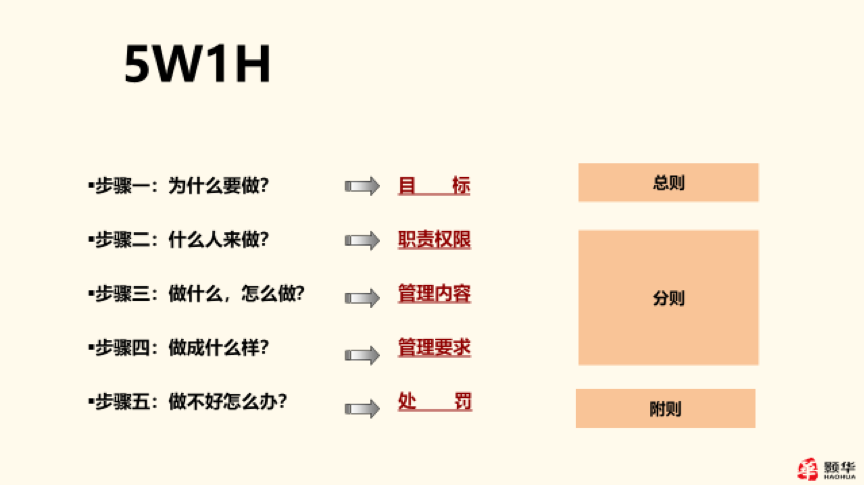
例如,小赵是个新员工,看到公司工作制度上规定:由自己部门负责编制项目立项申请,然后交由领导审批。于是他把自己的申请编制好后,拿给自己的直属部门领导审批,结果领导告诉他,还要有相关协作部门的审核,由协作部门领导签字后再给自己部门的分管领导审批,于是,小赵又去找了协作部门的部门领导。领导拿到申请后,认为这个申请还要由协作部门的分管领导审核,协作部门审核的程序终于走完了,等小赵给自己部门分管领导审核时,分管领导又提出,还需要公司的总经理办公会和董事会进行审议,因此需要对申请材料进行补充。这样来回重复工作,制度规定不明确,工作效率可想而知,这种感觉是不是十分熟悉!制度没有分清职责,使得员工不清楚正确的审批程序。应该有哪些部门参与协作,找哪些领导审批,分管领导应该管理什么审批什么,哪些事项的审议或决议需要上总经理办公会、董事会或股东大会,需要有一个清楚明确的依据和标准。通过制度把部门内部的职责、主责部门的责任、协作部门的责任、领导的责任明确后,就会减少像小赵一样的新员工在执行工作时的困惑,提高办事效率。另一方面,企业的领导层知道自己的责任后,就会变被动为主动,主动进行管理,管理意识和水平也会逐渐提高。
所以,内控主要帮助我们明确在一项业务中,哪个部门负主要管理责任,哪些部门负协助责任。制度通过对责任的划分,细化主责部门主要管理什么,管理要求是什么,要达到什么效果;并且明确协作部门的职责和权限,这样部门间的协作才能更加紧密,整个企业的运作因而更顺畅。
四、管理问责案例—长生生物疫苗造假事件
案例简介:
(一)基本情况
2018年7月15日下午,国家药监局通报:根据举报线索,国家药品监督管理局在7月6日-8日前往长春长生生物科技有限责任公司,开展飞行检查,发现该公司冻干人用狂犬病疫苗生产存在记录造假等严重违反《药品生产质量管理规范》的行为。
2018年7月18日,吉林食药监对长春长生生产不合格百白破疫苗处以344万元行政罚款。
2018年7月23日,长春警方对长春长生违法违规生产狂犬病疫苗立案调查。习近平作出重要指示:立即调查事实真相,一查到底,严肃问责。国务院调查组赶赴吉林,调查长春长生违法违规生产狂犬病疫苗案件。
2018年7月24日,长春长生公司董事长高某芳等15人被刑拘。
2018年7月29日,长春警方提请检察院批捕长春长生董事长等18人。
2018年8月1日,国家药监局会同国家卫生健康委等部门组成核查组赴湖北,对2017年发现的武汉生物效价不合格百白破疫苗处置工作开展核查。
2018年8月15日,国务院调查组进一步查明,长春长生生产的效价不合格百白破疫苗另有247200支,销往山东、安徽。
(二)“疫苗案”问责名单
7名省部级官员涉“疫苗案”被问责:
金育辉(吉林省副省长,2017年4月起分管吉林省食品药品监管工作)予以免职;
李晋修(吉林省政协副主席,2015年12月-2017年4月任分管吉林省食品药品监管工作的副省长)责令辞职;
要求刘长龙(长春市市长,2016年9月任长春市代市长,2016年10月至今任长春市市长)、毕井泉(市场监管总局党组书记、副局长,2015年2月-2018年3月任原食品药品监管总局局长)引咎辞职;
要求姜治莹(吉林省委常委、延边朝鲜族自治州委书记,2012年3月-2016年5月任长春市委副书记、市长)、焦红(国家药监局局长)作深刻检查;
中央纪委国家监委对吴浈(原食品药品监管总局副局长、原卫生计生委副主任,分管药化注册管理、药化监管和审核检验等工作)进行立案审查调查;
对35名非中管干部进行问责;
责成吉林省委和省政府、国家药监局向中共中央、国务院作深刻检查。
案例分析:
长生生物疫苗案,总体而言是由于“疫苗生产企业逐利,监管部门失职失察”所引发的。地方政府和监管部门监管责任落实不到位,导致问题疫苗猖獗,公共卫生安全底线失守。
管理思路:
管理机构被严厉的处罚,管理机构必须承担管理职责。政府与监管机构需要完善法律法规和制度规则,明晰和落实监管责任,加强生产过程现场检查,督促企业履行主体责任义务,建立质量安全追溯体系,落实产品风险报告制度。对风险高、专业性强的疫苗药品,需明确监管事权,在地方属地管理的基础上,要派出机构进行专项检查。同时加强监管队伍能力建设,尽快建设职业化、专业化的疫苗药品检查队伍。